Имплантат узнаёт и отбирает клетки из кровотока
Представьте себе мелкое терапевтическое устройство, помещённое в кровоток, которое отбирает из него определённые клетки и накапливает их либо им некоторый химический сигнал. Неужто снова нанобот? Нет.
Перед нами продукт биоинженерии: виртуозная комбинация верных веществ в верном месте.
Серийный аппарат, пока не имеющий какого-либо особого заглавия, проектируется с таким расчётом, дабы он умел определять в кровотоке целевые клетки (это смогут быть клетки иммунной совокупности, раковые либо стволовые клетки) и проводить с ними нужные манипуляции. Устройство должно отправлять отобранным клеткам некие команды (при помощи химических сигналов), захватывать необходимые для применения в другом месте (либо для «перепрограммирования»), либо кроме того уничтожать раковые.
Это необычное устройство возможно выполнено в виде некоего микроскопического объекта, введённого в сосуд, или как шунт, через что направляется поток крови. Оно должно оказать помощь медикам в лечении многих болезней, либо в их диагностике.
Наряду с этим «клеточный селекционер» обязан выпускаться серийно.
Такова храбрая цель американской компании CellTraffix, которая и финансирует данное изучение группы учёных. Главные фигуры проекта: Майкл Кинг (Michael King) из университета Рочестера (University of Rochester), являющийся кроме этого научным консультантом CellTraffix и автором устройства выборочного захвата клеток из кровотока, Джеффри Карп (Jeffrey Karp) из отделения медицинских технологий и наук Гарварда-МТИ (Harvard-MIT Health Sciences and Technology) и Сынпхё Хон (Seungpyo Hong) из Массачусетского технологического университета (MIT).
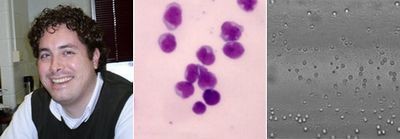
Майкл Кинг.
Справа: комплект снимков, показывающих кое-какие из его прошлых опытов по сбору определённых клеток при помощи устройства с покрытием из селектина (фотографии с сайта rochester.edu).
Думается, что для обнаружения в потоке клеток нужного типа микромашине потребуется что-то наподобие ИИ. Но нет, механизм селекции клеток тут основан только на биохимии.
Авторы данной совокупности решили имитировать в неестественном аппарате природный процесс, идущий в отечественных капиллярах и собственных сосудах. Его именуют «перекатка клеток» (cell rolling), а содержится он в том, что вблизи стенок сосуда определённые клетки быстро замедляются и начинают прокатываться на протяжении стены, а иногда — останавливаются.
Что происходит наряду с этим? Тут трудится вовсе не физическое трение, а своеобразные белки, именуемые селектины (P- и E-селектины, и другие).
Их в определённых обстановках начинают производить клетки эпителия, выстилающие стены сосуда. Селектины содержат молекулярные структуры, комплиментарные структурам на поверхности тех клеток крови, которых эти белки должны вылавливать из кровотока.
За счёт химических связей между этими структурами и происходит приклеивание.
Джеффри Карп (фото с сайта mit.edu).
А дальше? К примеру, определённый селектин начинают выделять сосуды, находящиеся в ткани, заражённой заразой. Появлявшиеся рядом лейкоциты связываются с этими веществами, останавливаясь у стены сосуда.
А тут уже белая клетка крови покидает русло, попадая в смежную с сосудом ткань, что и требуется для защиты органа от заразы.
Кинг сделал вывод, что в случае если обучиться воспроизводить таковой захват клеток из потока, возможно будет после этого делать с этими клетками что потребуется — хоть руководить их работой, хоть . Дабы проверить, как это будет трудиться, несколько Карпа нанесла на поверхность стекла P-селектин и разрешила войти по стеклу раствор с клетками.
Как и следовало ожидать, селектин начал вылавливать из потока те клетки, на каковые он был вычислен.
Увы, такое протеиновое покрытие оставалась стабильным только пара часов, а после этого разрушалось. В имплантате же захват клеток обязан трудиться семь дней а также месяцы, в противном случае больным будет необходимо всегда наведываться в госпиталь для замены устройства.
Выход был отыскан совсем сравнительно не так давно. Оказалось, что хорошую адгезию селектина к стеклу снабжает полиэтиленгликоль (PEG). Наряду с этим данное вещество не реагирует с другими белками и не захватывает их.
Для имплантата – то что необходимо.
Микросферы, снабжённые «лучами» — своеобразными молекулами, прокатываются по поверхности устройства, складывающегося из подложки (внизу) и закреплённого на ней белка-селектина (красные дуги) (иллюстрация Seungpyo Hong, MIT)
Для опробования нового покрытия несколько Карпа создала стеклянные микросферы, снабжённые «по кругу» молекулами, связывающимися с P-селектином. Эти микросферы играли роль целевых клеток крови.
Поток с этими шариками пускали на протяжении поверхности стекла, обработанного селектином и полиэтиленгликолем. Шарики быстро тормозились и начинали катиться, опираясь на селектин.
Причём данный эффект оставался стабильным в течение четырёх недель постоянного теста.
Сынпхё Хон (фото с сайта mit.edu).
Потом учёные удостоверились в надежности устройство захвата на клетках-нейтрофилах (это разновидность лейкоцитов). Покрытие кроме этого удачно отработало весь месяц.
Подробности собственных опытов учёные изложили в статье в издании Langmuir.
Следующий ход исследователей — добавление к связке PEG-селектин терапевтических агентов, взаимодействующих с отобранными клетками.
Таким своеобразным агентом, при необходимости, возможно соединение, являющееся для клетки знаком, что активирует апоптоз – суицид клетки. И в случае если устройство захвата будет ловить раковые клетки, распространяющиеся по кровотоку — таковой имплантат сможет очищать от них кровь, тормозя либо останавливая развитие ужасной заболевании.
Принцип уничтожения раковых клеток (продемонстрированы зелёным) новым устройством: селектин (Y), замедляет клетки в кровотоке.
Раковые клетки наряду с этим попадают к стенке устройства, где вступают в контакт со своеобразной молекулой (светло синий треугольник), включающей в клетке апоптоз, в следствии чего та погибает за 2-4 дня. Стрелками продемонстрирован перекатка и кровоток клеток (иллюстрация с сайта rochester.edu).
Второй вариант выполнения разрешит проводить клеточную терапию: устройство распознает в кровотоке стволовые клетки и подаст им сигнал на разделение в определённый тип. Либо их для извлечения, внедрения и очищения в другом месте, тому же больному.
Сейчас эту концепцию предстоит проверить в опытах на животных. И первые такие опыты, с имплантацией прототипа устройства живым крысам, уже выполнены.
Как информирует CellTraffix, возможность захвата стволовых клеток взрослой особи прямо из её кровотока доказана. Соответственно, сделан ещё один шаг на встречу к появлению новой разработке на рынке и к созданию многих родственных устройств, каковые отыщут себе работу в биологических исследованиях и медицине.



